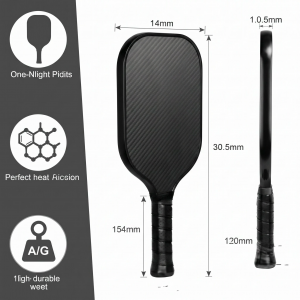
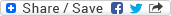Struktuur en eienskappe van koolstofvesel
Datum :2022-05-28 Bron: Fiber Composites
Die roosterstruktuur van die ideale grafietkristal behoort aan die seskantige kristalstelsel, wat 'n meerlaag-oorvleuelende struktuur is wat bestaan uit koolstofatome in 'n sesledige ringnetwerkstruktuur. In die sesledige ring is die koolstofatome in die vorm van sp 2 baster
Basiese struktuur
Die roosterstruktuur van die ideale grafietkristal behoort aan die seskantige kristalstelsel, wat saamgestel is uit koolstofatome wat uit 'n sesledige ringnetwerkstruktuur saamgestel is. In die sesledige ring, die koolstofatome is sp 2 hibridisasie bestaan. In sp2 hibridisasie is daar 1 2s elektron en 2 2p elektron hibridisasie, wat drie ekwivalente o sterk bindings vorm, die bindingsafstand is 0.1421nm, die gemiddelde bindingsenergie is 627kJ/mol en die bindingshoeke is 120 mekaar.
Die oorblywende suiwer 2p-orbitale in dieselfde vlak is loodreg op die vlak waar die drie o-bindings geleë is, en die N-bindings van die koolstofatome waaruit die N-binding bestaan is parallel aan mekaar en oorvleuel om 'n groot N te vorm -binding; Die nie-gelokaliseerde elektrone op die n-elektron kan vrylik parallel met die vlak beweeg, wat dit geleidende eienskappe gee. Hulle kan sigbare lig absorbeer, wat grafiet swart maak. Die van der Waals-krag tussen die grafietlae is baie minder as die valensbindingskrag binne die lae. Die spasiëring tussen die lae is 0,3354nm, en die bindingsenergie is 5,4kJ/mol. Die grafietlae word deur die helfte van die seskantige simmetrie verspring en in elke ander laag herhaal, wat ABAB vorm.
Struktuur [4], en beklee dit met selfsmeer en tussenlaag interne vermoë, soos getoon in Figuur 2-5. Koolstofvesel is 'n mikrokristallyne klip-inkmateriaal wat uit organiese vesel verkry word deur verkoling en grafitisering.
Die mikrostruktuur van koolstofvesel is soortgelyk aan dié van kunsmatige grafiet, wat tot die struktuur van polikristallyne chaotiese grafiet behoort. Die verskil van die grafietstruktuur lê in die onreëlmatige translasie en rotasie tussen die atoomlae (sien Figuur 2-6). Die ses-element netwerk kovalente binding is gebind in die atoomlaag van - wat basies parallel aan die vesel-as is. Daarom word algemeen geglo dat koolstofvesel saamgestel is uit 'n wanordelike grafietstruktuur langs die hoogte van die vesel-as, wat 'n baie hoë aksiale trekmodulus tot gevolg het. Die lamellêre struktuur van grafiet het beduidende anisotropie, wat maak dat sy fisiese eienskappe ook anisotropie toon.
Eienskappe en toepassings van koolstofvesel
Koolstofvesel kan verdeel word in filament, stapelvesel en stapelvesel. Die meganiese eienskappe word verdeel in die algemene tipe en hoë-prestasie tipe. Die algemene koolstofveselsterkte is 1000 MPa, die modulus is ongeveer 10OGPa. Hoëprestasie-koolstofvesel word verdeel in hoësterktetipe (sterkte 2000MPa, modulus 250GPa) en hoëmodel (modulus bo 300GPa). Sterkte groter as 4000MPa word ook ultra-hoë sterkte tipe genoem; Diegene met 'n modulus groter as 450GPa word ultrahoë modelle genoem. Met die ontwikkeling van die lugvaart- en lugvaartbedryf het koolstofvesel met 'n hoë sterkte en 'n hoë verlenging verskyn, en die verlenging daarvan is meer as 2%. Die groot hoeveelheid is polipropileen oog PAN-gebaseerde koolstofvesel. Koolstofvesel het hoë aksiale sterkte en modulus, geen kruip, goeie moegheidsweerstand, spesifieke hitte en elektriese geleidingsvermoë tussen nie-metaal en metaal, 'n klein termiese uitsettingskoëffisiënt, goeie korrosiebestandheid, lae veseldigtheid en goeie X-straal-oordrag. Die impakweerstand daarvan is egter swak en maklik om te beskadig, oksidasie vind plaas onder die werking van sterk suur, en metaal karbonisasie, karbonisering en elektrochemiese korrosie vind plaas wanneer dit met metaal gekombineer word. As gevolg hiervan moet koolstofvesel voor gebruik oppervlak behandel word.